A hét kísérlete !!! 
MOLEKULASEBESSÉG MÉRÉSE
Széntetraklorid molekulák átlagsebességének nagyságrendi becslése:
A mérés azon alapul, hogy a folyadékok párolgásakor v sebességgel kilépõ molekulák az impulzus-megmaradás törvénye értelmében visszalökõ erõvel hatnak a folyadékra. Érzékeny mérleggel kimutatható, hogy a széles nyitott edénybõl szabadon párolgó folyadék kissé nehezebb, mint a zárt edényben lévõ ugyanolyan mennyíségû folyadék.
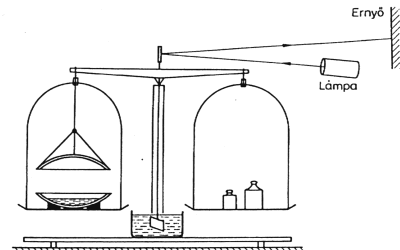
Egy 10 mg érzékenységû táramérleg egyik serpenyõjébe helyezzünk egy 6-8 cm átmérõjû óraüveget, és peremét - késõbbi okból - kenjük be vazelinnel. Egy hasonló nagyságú óraüvegre pecsétviasszal ragasszunk felfüggesztõ fonalat, és lógassuk az üveget a mérleg karjára kb. 5 cm magasan az elsõ óraüveg fölé. A mérleg mutatójára - csillapítás céljából - erõsítsünk egy kb. 5...10 cm2 felületû vékony rézlemezt, és merítsük olajjal vagy glicerinnel töltött edénybe. A mérlegkar tetejére ragasszunk fel viasszal egy kis tükröt, és világítsuk meg úgy, hogy a visszaverõdõ nyaláb egy kb. 3-4 m távolságban levõ ernyõre essék. A fénymutató érzékenyen jelzi a mérlegkar elmozdulását. Az így összeállított kísérleti berendezést a fenti. ábra szemlélteti.Töltsünk az alsó óraüvegbe széntetrakloridot és takarjuk le a felsõ óraüveggel! Tárázzuk ki a mérleget, majd vegyük le és akasszuk vissza a helyére a fedõként használt óraüveget! Rövid várakozási idõ után a megzavarás okozta billegés lecsillapodik. Az eredetileg kitárázott mérleg egyensúlya azonban állandóan változik, mert a párolgás miatt egyre könnyebbé váló serpenyõ lassan emelkedik. A mérleg lassú mozgását a fénymutató érzékenyen jelzi.
Jelöljük meg a fénymutató helyzetét és egyidejûleg indítsunk el egy stopperórát! Mérésünk tartson például 4*30=120 másodpercig! Jelöljük meg az egyre lejjebb vándorló fénymutató pillanatnyi helyzetét a 30., a 60. és a 90. másodpercben! A jelek kb. egyenlõ távolságra esnek egymástól. Ezután óvatosan arretáljuk a mérleget, majd a 120. másodpercben a felsõ óraüveggel fedjük le az alsót, és hozzuk a mérleget ismét lengõképes állapotba (dezarretáljuk)! Az egyensúly beállta után ismét jelöljük meg a fénymutató helyzetét!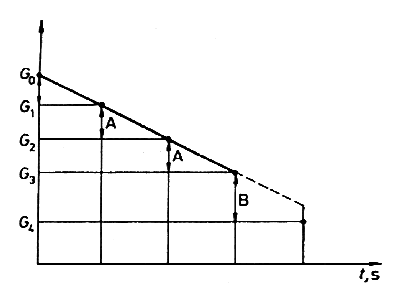
A mellékelt ábra a fénymutató helyzetét tünteti fel a 30 másodperces idõtartamok végén. A fénymutató helyzetének változása a mérleg serpenyõjére ható erõ változását mutatja.
Az elsõ három idõszakasz során a mérleg által jelzett erõ egyenletesen csökken, a negyedik periódus végén azonban a már letakart edény könnyebb annál, mint amilyennek a megelõzõ három mérés alapján lennie kellene. Az eltérést a molekuláknak a párolgás során a folyadékra gyakorolt F nyomóereje okozza, amibõl a molekulák átlagos sebessége megbecsülhetõ.A mérés kiértékelése:
Írjuk fel rendre a mérés kezdetén, illetve a 30 másodperces idõszakaszok végén a mérleg serpenyõjére ható G erõt!ahol Go, G1......G4 a serpenyõre ható erõ, Mo a folyadék kezdeti tömege; DM a 30 másodpercenként elpárolgó folyadék tömege, F a molekulák által kifejtett nyomóerõ. A fénymutató elmozdulása az elsõ három idõszakasz végén azonos (A), ez a mérleg tányérjára ható erõto=0 Go=Mog+F
t1=1Dt G1=(M1-1DM)g+F
t2=2Dt G2=(M2-2DM)g+F
t3=3Dt G3=(M3-3DM)g+F
t4=4Dt G4=(M4-4DM)gmegváltozásával arányos. Az utolsó 30 másodperc végén a párolgás megszûnt. A folyadékot letakartuk. A fénymutató ezután mért B elmozdulása aGo-G1=G1-G2=G2-G3=DMgerõváltozással arányos.G3-G4=DMg+F
Mindezek alapján az alábbi egyenlõségeket írhatjuk fel:ahol a C arányossági tényezõ az összeállítás geometriájától függõ állandó. A fenti két egyenlõség segítségével F értéke azA=CDMgB=C(DMg+F)
alakban fejezhetõ ki.F=(B/A - 1)DMg
Az F erõ molekuláris szinten a következõképpen értelmezhetõ: Jelölje 2N a folyadékfelszínbõl t idõ alatt kilépõ molekulák számát. Ezeknek mintegy a fele (N db) a gáztér részecskéivel történt ütközések hatására ismét a folyadékfelszínnel ütközik és visszajut a folyadékba. Belátható, hogy a molekulák azonos <v> átlagsebességgel lépnek ki, illetve csapódnak vissza a folyadékba. A t idõ alatt a folyadéknak ilyen módon átadott összes impulzus
ahol m egy molekula tömegét jelöli. Az elsõ tag a visszalökõdésbõl, a második a becsapódásból származik. A folyadékra kifejtett erõ az I impulzus felületre merõleges In komponensével az impulzustörvény alapján azI=2Nm<v>+Nm<v>=3Nm<v>alakban adható meg. Az In felületre merõleges impulzuskomponens meghatározásához figyelembe kell vennünk, hogy a kilépõ, illetve becsapódó molekulák sebessége egyenlõ valószínûséggel mutat a féltér minden irányába. Itt nem részletezett számítások szerint a molekulák eredõ impulzusának a folyadékfelszínre merõleges komponenseF= In/DtA párolgó folyadék látszólagos F súlynövekedése tehátIn=I/2A széntetraklorid molekulák <v> átlagsebessége az (1) és (2) formulák egybevetésével adható meg, ha figyelembe vesszük, hogy M=N.mF=(3Nm<v>)/(2Dt)
továbbá a B/A arány mérésünkbõl adódó értékét.Megjegyzések:<v> = (2/3)gDt(B/A - 1)- A mérés közben ügyeljünk arra, hogy a párolgás egyenletességét ne zavarja légáramlás, mert ez nagyságrendi hibát okozhat a molekulasebesség becslésében.
- A folyadék lefedésekor ügyeljünk a légmentes zárásra, ezt segíti az óraüveg szélére kent vazelin is.